Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
 Re
Re橋本 和幸; Wan, K. W. H. B. B.*; 松岡 弘充
Journal of Nuclear and Radiochemical Sciences, 6(3), p.193 - 196, 2005/12
治療に有効な核的特性を有するラジオアイソトープ(RI)をがんへ集積する性質を有する生理活性物質(モノクローナル抗体等)に標識した化合物は、がんの内用放射線治療への応用が期待されている。メルカプトアセチルトリグリシン(MAG3)は、生理活性物質のRI標識に有用な二官能性配位子の一つである。本研究では、がん治療に有効な核的特性を有するジェネレータ製無担体 ReによるMAG3標識について、直接合成法及び中間体を生成させるtransfer配位子(クエン酸及びグルコン酸)を用いた合成法による標識条件(Reの還元剤である塩化スズ濃度,pH,MAG3濃度,transfer配位子濃度,担体の有無等)の違いを詳細に比較検討した。最適条件下では、いずれの方法によっても90%以上の標識率が得られた。直接法とtransfer配位子法を比較すると、直接法は、反応を窒素気流中で行い、さらに溶媒の除去操作が必要であるが、transfer配位子法では必要がない。したがって、操作上は、transfer配位子法の方が簡便である。また、transfer配位子の違いにより、標識率のpH依存性の違いや室温での反応性の違いなどが観察された。今後は、transfer配位子の違いによる抗体標識及びtransfer配位子を利用した他の有用配位子の標識に関する検討を行う予定である。
ReによるMAG3標識について、直接合成法及び中間体を生成させるtransfer配位子(クエン酸及びグルコン酸)を用いた合成法による標識条件(Reの還元剤である塩化スズ濃度,pH,MAG3濃度,transfer配位子濃度,担体の有無等)の違いを詳細に比較検討した。最適条件下では、いずれの方法によっても90%以上の標識率が得られた。直接法とtransfer配位子法を比較すると、直接法は、反応を窒素気流中で行い、さらに溶媒の除去操作が必要であるが、transfer配位子法では必要がない。したがって、操作上は、transfer配位子法の方が簡便である。また、transfer配位子の違いにより、標識率のpH依存性の違いや室温での反応性の違いなどが観察された。今後は、transfer配位子の違いによる抗体標識及びtransfer配位子を利用した他の有用配位子の標識に関する検討を行う予定である。
小川 数馬*; 向 高弘*; 荒野 泰*; 小野 正博*; 花岡 宏史*; 石野 誠悟*; 橋本 和幸; 西村 洋*; 佐治 英郎*
Bioconjugate Chemistry, 16(4), p.751 - 757, 2005/07
被引用回数:61 パーセンタイル:86.86(Biochemical Research Methods)患者のQOL(生活の質)の向上を目指した癌性骨転移の疼痛緩和薬剤として、ビスホスホネート化合物の一つであるHEDPに 線を放出する
線を放出する Reを標識した
Reを標識した Re-HEDP化合物が検討されているが、血液クリアランスの遅さや胃への高い集積などが問題となっている。これはおもに、
Re-HEDP化合物が検討されているが、血液クリアランスの遅さや胃への高い集積などが問題となっている。これはおもに、 Re-HEDPが多核錯体であり、体内で不安定であるためであると考えられている。そこで、本研究では、二官能性放射性医薬品の概念に基づき、安定な
Re-HEDPが多核錯体であり、体内で不安定であるためであると考えられている。そこで、本研究では、二官能性放射性医薬品の概念に基づき、安定な Re単核錯体である
Re単核錯体である Re-MAG3(メルカプトアセチルトリグリシン)をビスホスホネート骨格を持つ化合物に導入した新規薬剤
Re-MAG3(メルカプトアセチルトリグリシン)をビスホスホネート骨格を持つ化合物に導入した新規薬剤 Re-MAG3-HBPを設計・合成し、その特性を調べた。その結果、MAG3-HBPと
Re-MAG3-HBPを設計・合成し、その特性を調べた。その結果、MAG3-HBPと Re標識クエン酸の配位子置換反応により、
Re標識クエン酸の配位子置換反応により、 Re-MAG3-HBPを95%以上の放射化学的純度で合成できた。また、本化合物は、リン酸緩衝溶液において、24時間後でも分解は観察されず、
Re-MAG3-HBPを95%以上の放射化学的純度で合成できた。また、本化合物は、リン酸緩衝溶液において、24時間後でも分解は観察されず、 Re-HEDPに比べてかなり安定であった。さらに、動物実験の結果、
Re-HEDPに比べてかなり安定であった。さらに、動物実験の結果、 Re-MAG3-HBPは、
Re-MAG3-HBPは、 Re-HEDPに比べて、高い骨への集積,速い血中クリアランス及び低い胃への集積を示し、癌性骨転移の疼痛緩和薬剤として優れた特性を有していることが明らかになった。
Re-HEDPに比べて、高い骨への集積,速い血中クリアランス及び低い胃への集積を示し、癌性骨転移の疼痛緩和薬剤として優れた特性を有していることが明らかになった。
山林 尚道
Japan-Russia Seminar on Utilization of Radiation and Radioisotopes for Medical Purposes, 0, p.1 - 12, 1994/00
原研では、放射線源として、がん治療のためのLDR(低線量率)用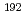 Ir小線源7種類、及び
Ir小線源7種類、及び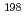 Au小線源7種類並びにHDR(高線量率)用
Au小線源7種類並びにHDR(高線量率)用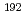 IrRALS(遠隔操作式治療装置)用の新しい治療用
IrRALS(遠隔操作式治療装置)用の新しい治療用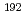 Ir線源及び骨密度診断用
Ir線源及び骨密度診断用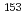 Gd線源の製造・開発を行っている。一方、がん治療用核医学薬品の原料として高比放射能
Gd線源の製造・開発を行っている。一方、がん治療用核医学薬品の原料として高比放射能 Cu,
Cu,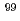 Moの他、近い将来疼痛軽減、治療にその利用が期待される
Moの他、近い将来疼痛軽減、治療にその利用が期待される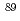 Sr,
Sr, Re及び
Re及び W/
W/ Reジェネレーターの製造・開発も進めている。これらの製造には、研究炉JRR-2(10MW),JRR-3M(20MW),JRR-4(3.5MW)及び材料試験炉JMTR(50MW)を利用している。
Reジェネレーターの製造・開発も進めている。これらの製造には、研究炉JRR-2(10MW),JRR-3M(20MW),JRR-4(3.5MW)及び材料試験炉JMTR(50MW)を利用している。
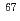 Cuの大量製造法の開発
Cuの大量製造法の開発橋本 和幸; 川端 方子*; 佐伯 秀也*; 佐藤 俊一*; 塚田 和明; 渡辺 智; 永井 泰樹
no journal, ,
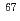 Cu(半減期61.9時間)は、がん治療に適した
Cu(半減期61.9時間)は、がん治療に適した 線(平均エネルギー141keV)と画像診断に適した
線(平均エネルギー141keV)と画像診断に適した 線(185keV等)を同時に放出するため、がん治療用核種として有望視され30年余にわたりその有効な生成法開発が模索されている。従来、
線(185keV等)を同時に放出するため、がん治療用核種として有望視され30年余にわたりその有効な生成法開発が模索されている。従来、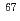 Cuを製造するには、高エネルギー陽子を用いた
Cuを製造するには、高エネルギー陽子を用いた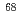 Zn(p,2p)
Zn(p,2p)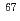 Cuが最適であると考えられているが、生成量が限られていることや副生成RIの多さ等の問題から、研究開発も限定的な状況である。そこで我々は、従来法に代わる製造法として、加速器からの高速中性子を用いた
Cuが最適であると考えられているが、生成量が限られていることや副生成RIの多さ等の問題から、研究開発も限定的な状況である。そこで我々は、従来法に代わる製造法として、加速器からの高速中性子を用いた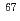 Cu製造法[
Cu製造法[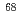 Zn(n,x)
Zn(n,x)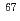 Cu反応(x=n'p, d)]の開発を行っており、ターゲット物質であるZn(5g ZnO)からの基本分離法を確立した。本研究では、実用化を目指す次のステップとして、副生成RIである
Cu反応(x=n'p, d)]の開発を行っており、ターゲット物質であるZn(5g ZnO)からの基本分離法を確立した。本研究では、実用化を目指す次のステップとして、副生成RIである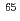 Ni(半減期2.52h)を新たに分離する高純度化手法及び大量製造化のためのZnO試料増量(基本分離法の5倍以上の試料量)に対応した分離・精製法を検討した。
Ni(半減期2.52h)を新たに分離する高純度化手法及び大量製造化のためのZnO試料増量(基本分離法の5倍以上の試料量)に対応した分離・精製法を検討した。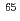 Ni分離手法の開発では、既報の基本分離法において、8M HClの追加使用及び陰イオン交換樹脂カラムのサイズアップを図ることにより、最終
Ni分離手法の開発では、既報の基本分離法において、8M HClの追加使用及び陰イオン交換樹脂カラムのサイズアップを図ることにより、最終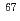 Cu溶液中の
Cu溶液中の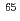 Ni残量は検出限界以下であり、
Ni残量は検出限界以下であり、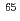 Ni分離手法を確立した。さらに、33g ZnO試料を用いた分離挙動を調べた結果、上記
Ni分離手法を確立した。さらに、33g ZnO試料を用いた分離挙動を調べた結果、上記 Ni分離を可能にした改良分離法により、CuとZnの分離は良好で、Cu最終溶液中に、
Ni分離を可能にした改良分離法により、CuとZnの分離は良好で、Cu最終溶液中に、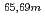 Znは検出されず、より高純度の
Znは検出されず、より高純度の Cuを製造する方法を確立した。
Cuを製造する方法を確立した。
 Cuの大量製造に関する検討
Cuの大量製造に関する検討橋本 和幸; 川端 方子*; 佐伯 秀也*; 佐藤 俊一*; 塚田 和明; 初川 雄一; 永井 泰樹; 渡辺 智; 石岡 典子
no journal, ,
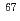 Cu(半減期62時間)は、がん治療に適したベータ線(平均エネルギー141keV)と画像化に適した
Cu(半減期62時間)は、がん治療に適したベータ線(平均エネルギー141keV)と画像化に適した 線(185keV)を同時に放出するため、がん治療用核種として有望視されている。しかし、大量に高品質の
線(185keV)を同時に放出するため、がん治療用核種として有望視されている。しかし、大量に高品質の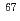 Cuを製造する方法が限られているため、研究開発が限定的である。そこで我々は、AVFサイクロトロンにて重陽子ビームを炭素あるいはベリリウム標的に照射することで発生する高速中性子を
Cuを製造する方法が限られているため、研究開発が限定的である。そこで我々は、AVFサイクロトロンにて重陽子ビームを炭素あるいはベリリウム標的に照射することで発生する高速中性子を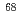 ZnOに照射することにより
ZnOに照射することにより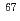 Cuを製造する手法の開発を行っている。本研究では、動物実験が可能な放射能量の
Cuを製造する手法の開発を行っている。本研究では、動物実験が可能な放射能量の Cuを製造するための分離手法の検討を行った。まず、ターゲット物質であるZnO増量(5g
Cuを製造するための分離手法の検討を行った。まず、ターゲット物質であるZnO増量(5g 33g)に対応する分離手法の開発では、33g ZnO試料を用いた場合でも、既報の基本分離法を用いることにより、CuとZnの分離は良好であり、Cu最終溶液中に、
33g)に対応する分離手法の開発では、33g ZnO試料を用いた場合でも、既報の基本分離法を用いることにより、CuとZnの分離は良好であり、Cu最終溶液中に、 Znは検出されなかった。また、濃縮
Znは検出されなかった。また、濃縮 ZnOターゲットの回収方法として、キレート樹脂カラムから溶出されるZn溶液を水酸化物沈殿法により分離回収する方法を検討した結果、回収したZnOには、標識を阻害する新たな不純物の混入は認められなかった。以上の結果、既存加速器を用いて動物実験が可能な数百MBqの
ZnOターゲットの回収方法として、キレート樹脂カラムから溶出されるZn溶液を水酸化物沈殿法により分離回収する方法を検討した結果、回収したZnOには、標識を阻害する新たな不純物の混入は認められなかった。以上の結果、既存加速器を用いて動物実験が可能な数百MBqの Cuを製造する手法の開発に目途が立った。
Cuを製造する手法の開発に目途が立った。